生物标记物解决方案,围绕您的需求设计
综合多学科的解决方案,可满足您的生物标记物策略目标
个性化生物标记物支持,可帮助推动您的研发工作从实验台迈向商业化
符合您独特要求的协作、科学设计和问题解决方法
深入的专业知识和洞见,可推动您的临床前和临床研究(包括探索性生物标记物计划),乃至实现商业化
创新、最尖端的平台和全球实验室测试能力

生物标记物是当今药物研发与个体化用药目标的核心,在2018年FDA审批中占比超过40%1。其有助于定义疾病生物学、推动患者识别和分层、识别作用机制并了解药物的药效以及其他方面。
高效药物研发的明确前进道路
如要完全实现生物标记物策略的优势,您需要早期洞见、专注的专业知识以及包括最先进技术和平台的清晰蓝图。首先要深刻了解生物标记物在方案中的作用、拟定的应用以及哪些工具将帮助您实现目标。
还必须考虑为您的生物标记物方案选择最合适的法规环境。快速研发、验证以及(必要时)转让您的测定法将优化您的时间安排和财务影响。
1个性化医学联盟。FDA个体化用药:进度与展望报告,2018
与您的分子一样独一无二的方案
在我们专注于关键治疗领域的生物标记物解决方案中心博士团队的领导下,您生物标记物方案的设计将依托涉及以下三个关键领域的行业洞察力和深厚专业知识:
生物标记物的作用
- 预测
- 药效学
- 监控
- 预后
- 安全性
- 易感性/风险
- 诊断
预期用途
- 作用机制识别
- 替代性终点
- 患者识别/分层
- 包含/排除
- 患者护理
- 伴随诊断
工具
- 下一代排序
- 流式细胞计量术
- 免疫组织化学
- 免疫测定法
- 基于细胞的测定法
- 液相色谱-质谱联用仪(LC-MS)
- 解剖病理学
这最终促成了全面考虑整个方案、平台以及按时完成里程碑的定制方案。
在科文斯和LabCorp中,广泛的全球实验室测试能力(从标准临床实验室和安全性测试到深奥和复杂的生物标记物测试)不仅构成超过4,500种分析方法,而且还具有为您的生物标记物研发新检测方法的能力。无论您的方案需要探索性/定制的检测方法,还是GLP/GCLP和CAP/CLIA规范的环境,您都可以随着法规要求的变化,高效地安排方案并经济有效地进行转让。
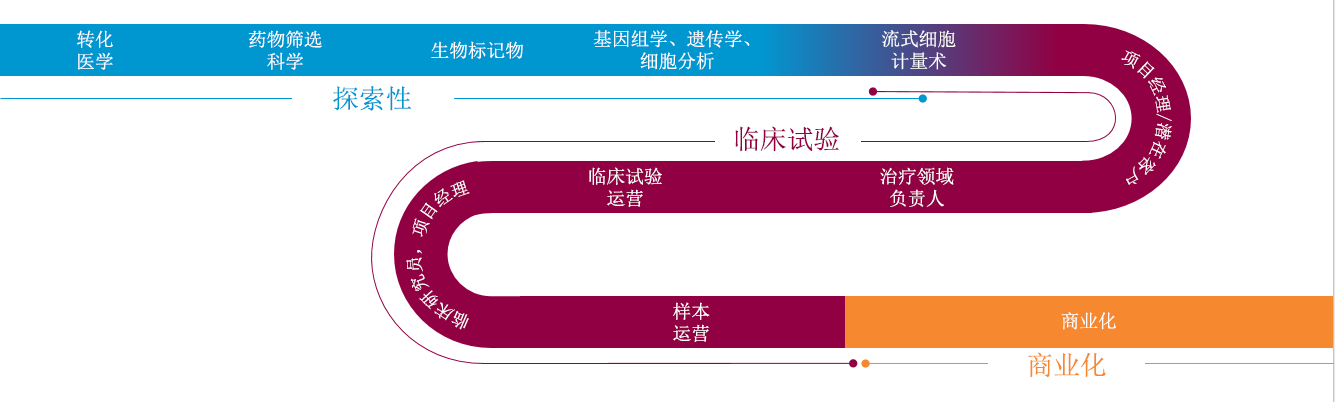
从实验台到商业化的生物标记物解决方案
了解整个药物研发进程是了解生物标记物数据的利用如何随着方案的成熟而变化,并且快速响应以保持遵守时间安排的关键。
无论您是正在积极规划伴随诊断注册试验,还是仍在试图确认您的生物标记物候选物可以预测治疗反应,全面审视整个诊断流程都能避免监管监督、数据完整性和研发时间安排方面的差距。
通过及早与科文斯诊断研发服务团队开展合作,可以获得药物和诊断联合研发领域从概念到商业化的行业领先的专业知识。