ID8:用于检测卵巢癌免疫疗法的同基因小鼠模型
ID8-Luc是一种用于治疗原位卵巢癌的新型同基因小鼠模型。卵巢癌仍然是一个重要的未满足的医疗需求,诊断为高度晚期四期卵巢癌患者的相对5年生存率为17%。
作者:
Dylan Daniel,博士,科学发展主任
日期:
2017年11月
卵巢癌是一种尚未得到满足的医疗需求,尤其致命,因为它往往只有在疾病相当严重时才会被发现。2017年,美国约有22,440名女性被诊断出卵巢癌,约有14,080人死亡。在美国,以铂和抗分裂紫杉烷为基础的联合化疗是标准的治疗方案,但尽管这些治疗方案在最初通常是有效的,但复发和进展通常发生。治疗卵巢癌需要新的治疗方法。
基于最近利用免疫系统治疗其他癌症的成功,药物研发科学家们探索了卵巢癌的免疫治疗方法。目前有超过50个临床试验测试卵巢癌的免疫治疗方法和组合;然而,有有限数量的同基因小鼠卵巢癌模型可用来实现临床前药理学。yaboapp体育官网Covance开发了ID8同基因小鼠细胞系模型,用于测试标准疗法以及免疫肿瘤学应用。ID8来源于体外连续传代转化的C57BL/6小鼠卵巢表面上皮细胞。1Luciferase was expressed in the ID8 cells (ID8-Luc-mCherry-Puro) to enable monitoring of orthotopic (intraperitoneal) tumor growth by bioluminescence imaging (BLI).
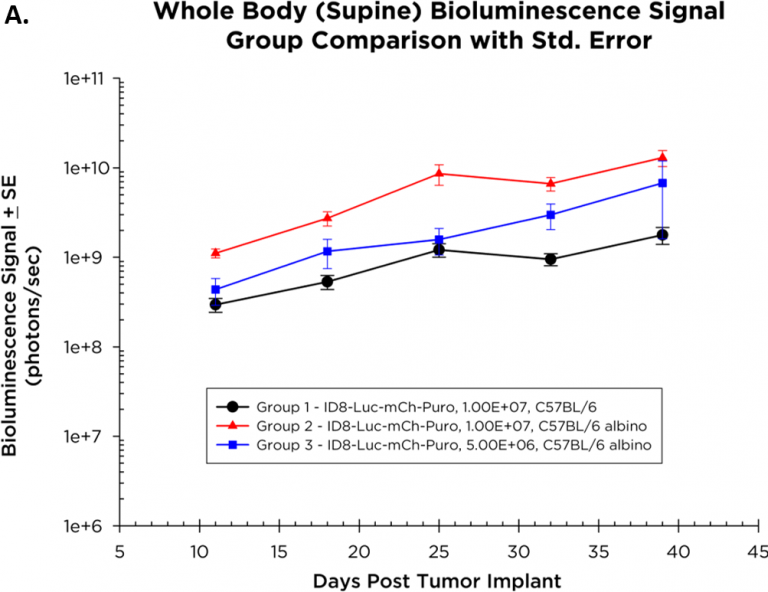
绘制了BLI监测id8 - lucc - mch - puro的平均肿瘤生长动力学(图1A)和个体生长动力学(图1B)。植入1.0×107每只小鼠产生的细胞比5.0×10的肿瘤生长更一致6C57BL/6白化病小鼠每只小鼠的细胞数。与预期的一样,C57BL/6白化小鼠(绿线,图1B,组2)的信号(光子/秒)比野生型C57BL/6小鼠(红线,图1B)的信号(光子/秒)更高,因为它们的皮肤中缺少吸收肿瘤细胞输出光的黑色素。id8 - lucch - puro原位疾病进展的代表性BLI图像如图1C所示。


小鼠ID8吕克-MCH-迪普罗细胞植入长胖在研究(图2)与只在研究结束一些小鼠显示体重损失的持续时间。疾病进展,表现为腹胀由于腹水形成(图3),是线性的与在C57BL的35-40天存活/ 6小白鼠植入1.0×107细胞。


Covance对携带id8 - lucc - mch - puro小鼠腹水进行免疫分析。在表1中,总CD45的免疫谱+白细胞,CD4+CD8 T细胞,+T细胞,调节性T细胞,M-MDSC,G-MDSC,M1 TAM和M2 TAM被示出。虽然在小鼠的免疫谱相当的异质性,所有小鼠有一个强劲的CD8+CD8良好的T细胞浸润+T细胞/ Treg比率。据报道,ID8卵巢癌模型对IL-12免疫治疗联合有利的CD8产生反应+T细胞/ Treg细胞比率表明该模型应该支持新型免疫疗法的测试。2研究,分析响应免疫治疗以及护理标准目前正在开发中。
表1:id8 - lucch - puro卵巢癌小鼠腹水单个小鼠免疫细胞亚群的流式细胞仪分析
* CD8 / Treg的比的基础上确定来自个体CD8和Treg栅极的绝对计数。
未确定
接触Covance与我们的一位科学家交谈,看看ID8或我们的其他同基因模型如何用于您的下一个免疫肿瘤学研究。
模型SPOTLIGHT | ID8同基因卵巢癌模型对检查点抑制剂的反应(PDF版本)
1罗比KF等人,针对与卵巢癌事件同基因小鼠模型的发展。致癌作用。2000,第21:585-591。
2Janat-Amsbury MM等人,在一种同基因ID8小鼠模型中,局部、非病毒IL12基因治疗和全身紫杉醇化疗相结合的人卵巢癌。《肿瘤研究》2006年第26卷第3223-3228页。
注:研究是在按照一个AAALAC认证的机构适用的动物福利法规进行
