Hepa 1-6: A murine model of hepatocellular carcinoma
肝细胞癌(hepatocellularcarcinoma,HCC)是一种侵袭性恶性肿瘤,其发病率逐渐上升,已影响到全世界100万人,是目前世界第三大癌症相关死亡原因。[1,2]由于乙型和丙型肝炎病毒的高度地方性,肝癌的发病率在亚洲和非洲最高,这极易发展为慢性肝病和随后的肝癌。[1]在西方人群中,丙型肝炎、酒精性肝硬化和非酒精性脂肪性肝炎(NASH)是主要的潜在原因。早期肝癌的治疗方案包括手术切除、肝移植、化疗/放疗栓塞和射频消融,晚期肝癌的治疗标准是靶向治疗(索拉非尼和雷戈拉非尼)、放疗和化疗(阿霉素、5-FU和顺铂)。[3]许多临床试验正在进行中的不可切除或晚期肝癌与单一或联合免疫治疗,单克隆抗体或溶瘤病毒治疗。[1-4]These therapies have demonstrated tumor shrinkage and improved survival but are not curative with the treatment outcome contingent on pre-existing conditions such as hepatitis, liver cirrhosis, or nonalcoholic fatty liver disease (NAFLD). Hence, there is an ever-increasing need for better treatment options. To evaluate novel therapies in a preclinical platform, Covance has established the syngeneic HCC model Hepa 1-6.
Hepa 1-6 is a murine hepatoma derived from the BW7756 hepatoma tumor that arose spontaneously in C57L/J mice, which contrasts with most available hepatoma models (BNL, A.7R.1, MH-129, MH134 and MH-22A) that are chemically transformed or induced lines. The Hepa 1-6 tumor model established in immunocompetent mice represents a clinically relevant model for preclinical testing of immunotherapy.
In this model spotlight we present体内关于hep1-6肿瘤模型生长动力学的数据;以及单独或联合局部辐射对检查点抑制剂的反应。我们在其亲本C57L/J菌株(在杰克逊实验室有限的可用性,巴尔港,ME)和更容易获得的组织相容性C57BL/6菌株中测试了该模型。
Hepa 1-6生长参数
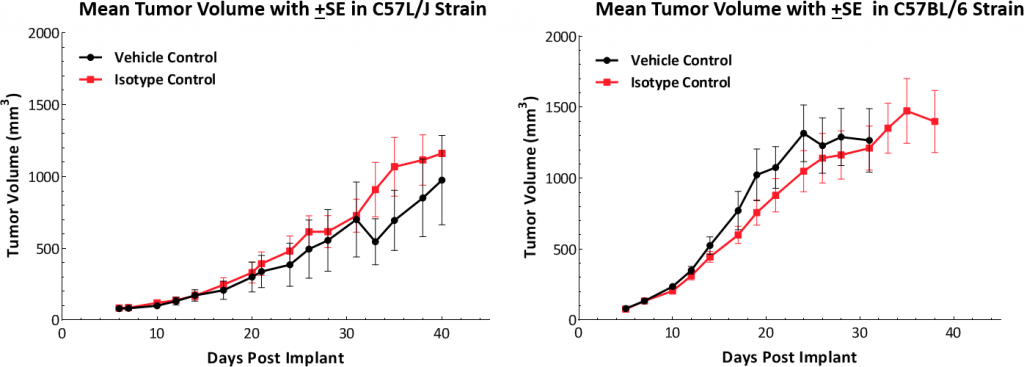
生长动力学皮下的植入物显示模型在两种小鼠品系中均成功建立(图1)。肿瘤的中位倍增时间约为5-6天,无不良体重变化(数据未显示)。这种稳定的生长速度为评估抗肿瘤反应提供了一个为期三周的治疗窗口。
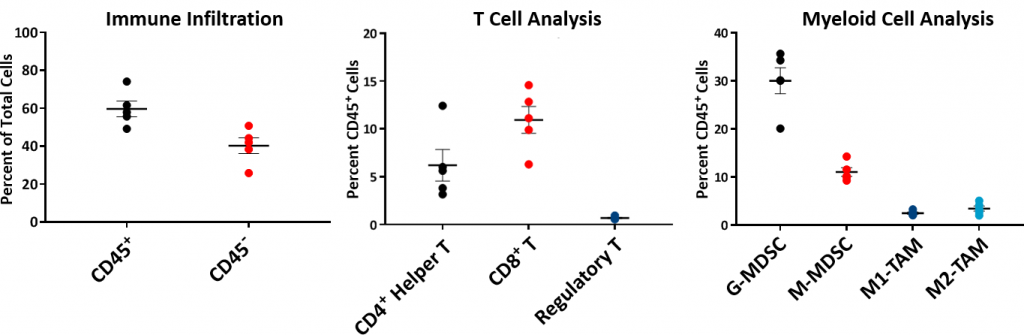
Hepa 1-6肿瘤免疫谱
To understand the immune profile of the Hepa 1-6 tumors, baseline immune composition was analyzed by流式细胞术and is shown in Fig. 2. The immune profile was established from five untreated Hepa 1-6 tumors grown in the C57L/J strain to ~750-1000mm3in volume. Tumors have a relatively high CD45+细胞群(平均约60%),其中T淋巴细胞(CD8+T细胞和CD4+辅助性T细胞(T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells,T-helper cells)的表达中等。骨髓细胞群主要为G-MDSC(平均约30%),其次为M-MDSC(平均约11%)。CD8+肿瘤微环境中的T细胞浸润提示一种免疫应答或“温热”肿瘤模型。
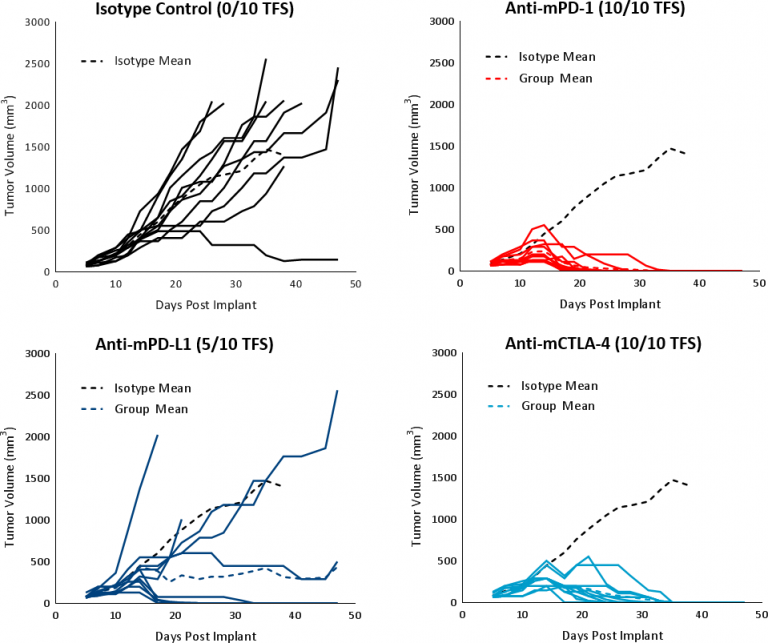
Hepa 1-6 Response to Checkpoint Inhibitors
hep1-6对免疫调节剂的反应在已建立的荷瘤(平均肿瘤体积~100mm)中进行评估3)用检查点阻断抗体(抗mPD-1、抗mPD-L1和抗mCTLA-4)治疗的C57BL/6小鼠。对照组,载体(PBS)和同种型(大鼠IgG2b克隆LTF-2)显示出相似的生长动力学(图1)。单药检查点抑制剂抗mPD-1和抗mCTLA-4引起强烈反应,导致肿瘤完全消退(CR)和100%无瘤生存(TFS)。抗mPD-L1治疗也在一部分动物中产生了良好的反应,导致CR和5/10 TFS(图3)。与对照组相比,用检查点抑制剂抗体治疗与任何显著的体重变化无关(数据未显示)。对免疫治疗的反应有力地支持了hep1-6肿瘤在免疫学上的“热”特征
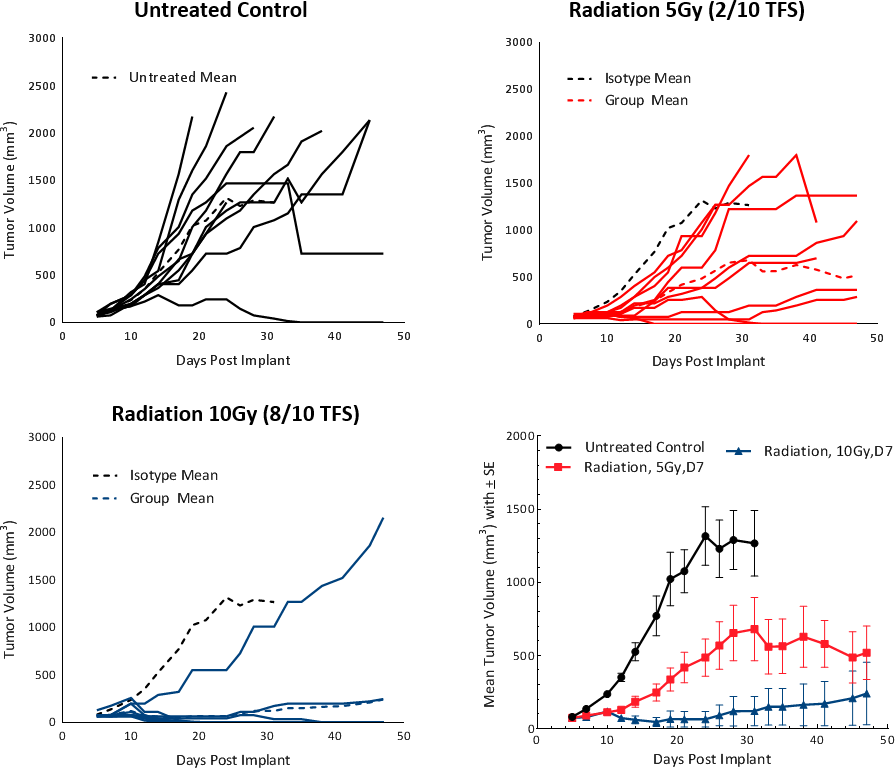
对焦辐射的反应
临床上,非转移性肝癌患者接受一种或多种肝脏导向治疗(LDT),如放射治疗(RT)或立体定向全身放射治疗(SBRT)。[5]RT can result in tumor shrinkage and alter the tumor microenvironment to a favorable tumor suppressive milieu. To test the response of Hepa 1-6 tumors to RT, we used the Small Animal Radiation Research Platform (SARRP; Xstrahl) to deliverfocal beam radiationto targeted areas. Focal radiation doses of 5 and 10Gy were tested on subcutaneous Hepa 1-6 tumors in C57BL/6 mice. Treatment showed a dose dependent response and resulted in >20 days tumor growth delay (TGD) and tumor free survivors (2/10 and 8/10, respectively) (Fig. 4). A dose of 5Gy provided a moderate monotherapy response with increased life span and is recommended for future combination studies.
Hepa 1-6对索拉非尼的反应
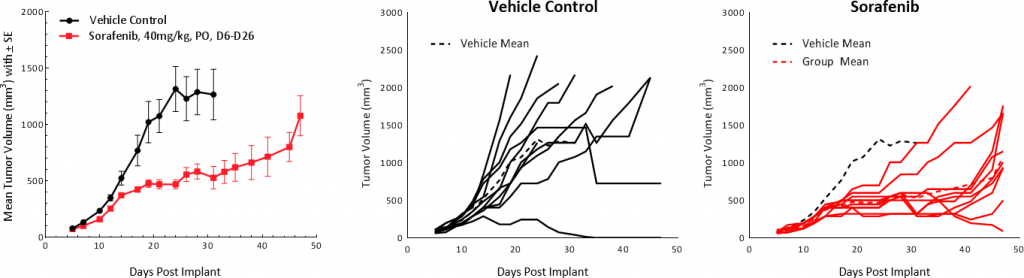
索拉非尼是一种阻断Raf激酶、Src、VEGF和PDGF受体活性的多酪氨酸激酶抑制剂,用于肝癌患者的一线治疗,在hep1-6肿瘤上进行了试验。治疗导致肿瘤生长延迟25.4天,延长了总生存期,但没有TFS(图5)。这些结果与临床研究的结果相当,临床研究显示部分缓解将中位总生存期从对照组的7.9个月延长到治疗组的10.7个月。[1]
These preliminary data suggest that the Hepa 1-6 model of HCC has a favorable immune profile and can be employed as a robust preclinical免疫肿瘤学模型。我们的数据支持使用该模型研究免疫治疗剂作为单一疗法或与辐射、小分子、护理标准和其他新疗法相结合。拜托联系人Covance与我们的科学家讨论如何将Hepa 1-6用于下一个免疫肿瘤学研究。
模型聚光灯| Hepa 1-6:小鼠肝细胞癌模型(PDF版本)
[1]Medavaram,S和Zhang Y,2018年。晚期肝细胞癌的新疗法。实验血液肿瘤学7:17。
[2]Llovet JM、Montal R、Sia D和Finn RS,2018年。肝细胞癌的分子治疗和精确医学。国家修订临床肿瘤学。内政部:10.1038/s41571-018-0073-4。[打印前电子出版]PMID:30061739。
[3]Pinter M&Peck Radosvljevic M.2018年。综述文章:肝细胞癌的系统治疗。2018营养药物疗法,7月23日。内政部:10.1111/apt.14913。[印刷前电子出版]回顾。PMID:30039640。
[4]Waidmann O.2018年。肝细胞癌免疫治疗的新进展。生物治疗专家。8月18日(8):905-910。
[5]Chaub SK等人,2018年。肝细胞癌立体定向全身放射治疗:当前趋势和争议。癌症研究与治疗技术17:1-19。
注:研究是根据适用的动物福利条例在AAALAC认可的机构中进行的