4T1-LUC2:一种原位乳腺癌模型,支持新型免疫肿瘤药物发现
乳腺癌是美国肺癌后肺癌最致命的恶性肿瘤,估计预计2016年的246,000例新病例和40,450人死亡。存在乳腺癌的许多治疗方案,包括手术,放射治疗,抗雌激素治疗,靶向治疗(e.g., trastuzumab), and chemotherapy. Despite these therapeutic advances, metastatic disease remains a significant source of mortality. Immunotherapy has seen remarkable progress in the last five years with four T cell immune checkpoint inhibitors approved. While none of these checkpoint inhibitors are approved in breast cancer, there are currently 60+ clinical trials ongoing in breast cancer with checkpoint inhibitors against PD-1 or PD-L1 and 20+ clinical trials ongoing with CTLA-4 inhibitors.
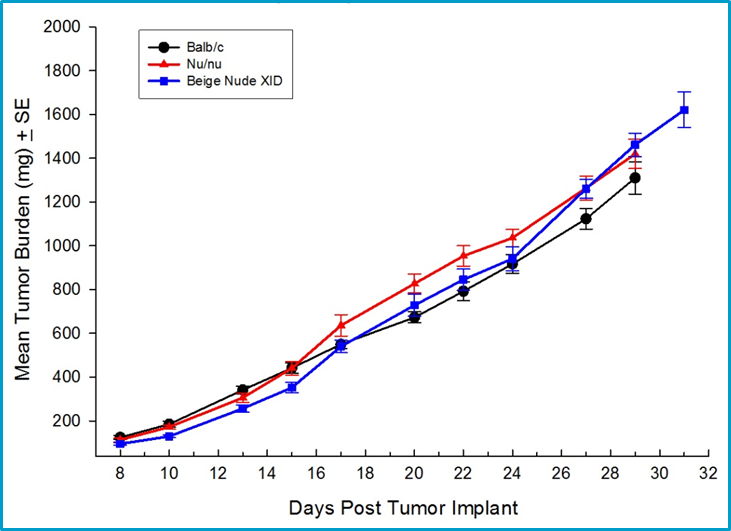
由于检查点抑制剂和其他类别免疫治疗需要完整的免疫系统来引发活性,因此乳腺癌的同胞小鼠模型是新型剂的临床前测试的重要选择。yaboapp体育官网Covance已经完全表征了来自Balb / C小鼠的4T1-Luc2乳腺癌模型,作为支持具有新型免疫肿瘤学剂的研究的原位模型。原位4T1-LUC2肿瘤转移到淋巴结和肺部,使其成为研究疗法对使用生物发光成像的原发性肿瘤和转移性疾病的效果。4T1-Luc2肿瘤的生长在免疫缺陷菌株和免疫竞争力的BALB / C小鼠中的增长,这表明4T1-LUC2是弱免疫原性肿瘤(图1)。
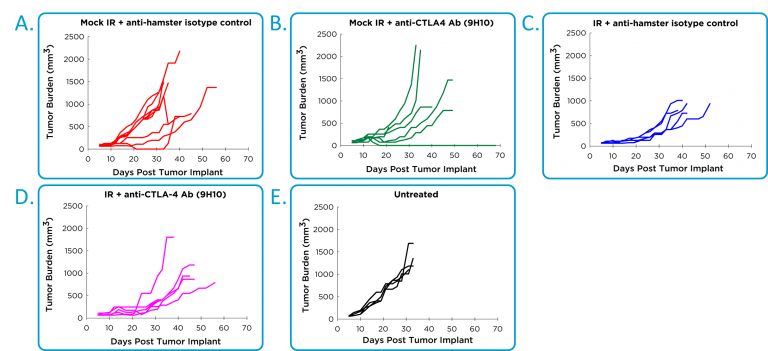
通过轴承4T1肿瘤的小鼠致命的超敏反应阻碍了对PD-1或PD-L1的抗体的功效研究。1可以在没有毒性的情况下给药两剂,但不可能给药。相反,评价抗CTLA-4与局部辐射组合的疗效。使用仓鼠抗CTLA-4抗体,并且出乎意料地将仓鼠同种型对照显示出在一些小鼠(图2A)中显示出显着的活性,其与抗CTLA-4活性难以区分(图2B)。与局部辐射有关的治疗益处(图2C),但没有明确改善辐射和抗CTLA-4的组合(图2D)。
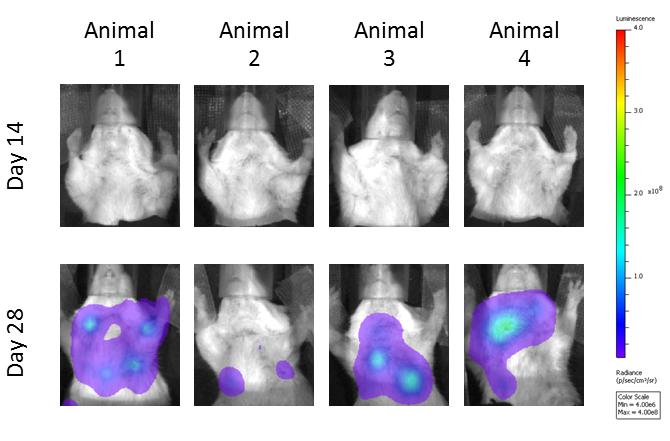
使用生物发光成像评估转移性负担,并且所示是未处理的小鼠中转移的转移进展的代表性图像(图3A)。抗CTLA-4处理的小鼠相对于同种型对照处理小鼠的转移性肿瘤负荷降低(图3B)。局部辐射也显着降低了转移负荷;然而,在组合组中的抗CTLA-4的单一代理活性似乎没有改善。
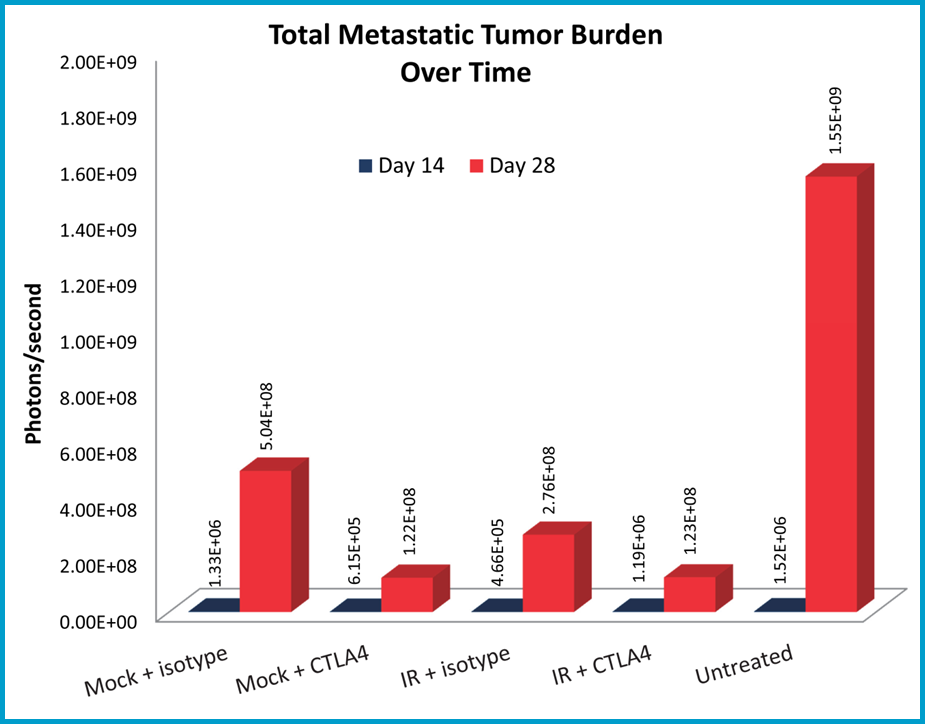
本研究中的辐射是使用引线屏蔽的定位,以减少总体辐射;然而,一些动物仍然显示出辐射毒性的迹象。Covance现在提供Xstrahl的小动物辐射研究平台(SARRP)提供焦束辐射能力,从而降低了系统辐射毒性。
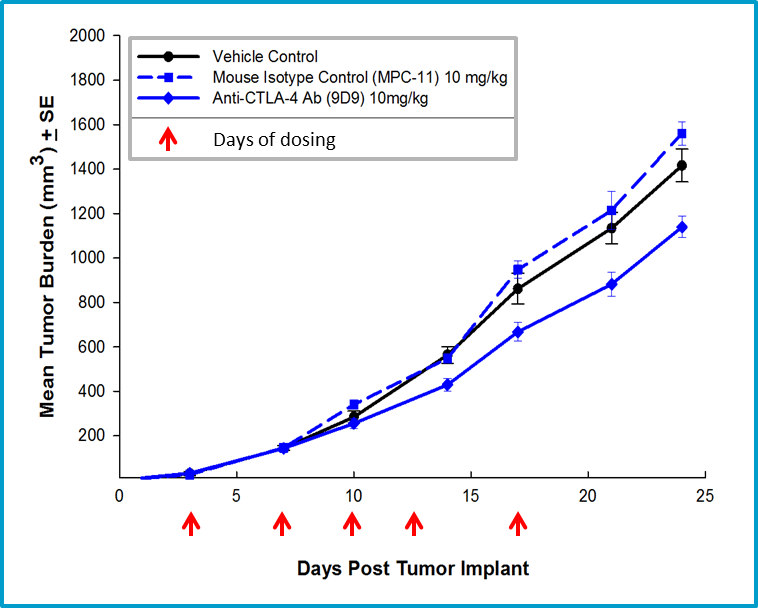
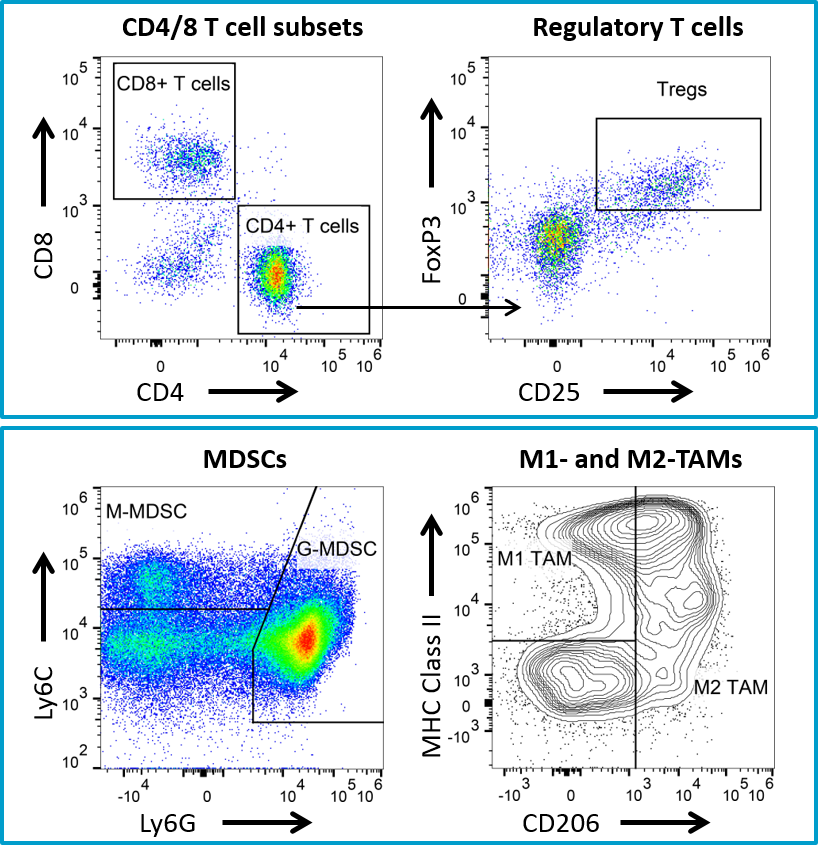
与使用4T1-LUC2模型中使用仓鼠抗体相关的非特异性抗肿瘤活性促使使用小鼠抗CTLA-4抗体进行后续研究。小鼠抗CTLA-4治疗导致4T1-LUC2模型中的最小活性(图4),但为客户提供了具有新型免疫脑病学剂的客户赞助研究的潜在组合合作伙伴。此外,我们有广泛的流式细胞仪免疫谱分析4T1-Luc2肿瘤,包括CD4 T细胞,CD8 T细胞,调节性T细胞,粒细胞-MDSC,单核细胞-MDSC,M1-和M2肿瘤相关巨噬细胞(TAMS)的定量(图5)。该模型具有很好的特征,可用于客户赞助的研究,该研究具有新的免疫疗法或可与市售免疫疗递相结合的药剂。请联系我们有关详细信息,并了解Covance如何帮助您的下一项研究。
1Mall等人。,oncoimmunology(2016),Vol。5(2):E1075114
注意:研究是根据AAALAC认可的设施中适用的动物福利法规进行的